ENZIMAS
Las enzimas[1]
son moléculas
de naturaleza proteica que catalizan
reacciones químicas, siempre que sean termodinámicamente
posibles: una enzima hace que una reacción química que es energéticamente
posible (ver Energía libre de Gibbs), pero que transcurre
a una velocidad
muy baja, sea cinéticamente favorable, es decir, transcurra a mayor velocidad
que sin la presencia de la enzima.[2]
[3]
En estas reacciones, las enzimas actúan sobre unas moléculas
denominadas sustratos, las cuales se convierten en
moléculas diferentes denominadas productos. Casi todos los procesos en las células
necesitan enzimas para que ocurran a unas tasas significativas. A las
reacciones mediadas por enzimas se las denomina reacciones enzimáticas.Debido a que las enzimas son extremadamente selectivas con sus sustratos y su velocidad crece solo con algunas reacciones, el conjunto (set) de enzimas presentes en una célula determina el tipo de metabolismo que tiene esa célula. A su vez, esta presencia depende de la regulación de la expresión génica correspondiente a la enzima.
Como todos los catalizadores, las enzimas funcionan disminuyendo la energía de activación (ΔG‡) de una reacción, de forma que la presencia de la enzima acelera sustancialmente la tasa de reacción. Las enzimas no alteran el balance energético de las reacciones en que intervienen, ni modifican, por lo tanto, el equilibrio de la reacción, pero consiguen acelerar el proceso incluso en escalas de millones de veces. Una reacción que se produce bajo el control de una enzima, o de un catalizador en general, alcanza el equilibrio mucho más deprisa que la correspondiente reacción no catalizada.
Al igual que ocurre con otros catalizadores, las enzimas no son consumidas en las reacciones que catalizan, ni alteran su equilibrio químico. Sin embargo, las enzimas difieren de otros catalizadores por ser más específicas. La gran diversidad de enzimas existentes catalizan alrededor de 4000 reacciones bioquímicas distintas.[4] No todos los catalizadores bioquímicos son proteínas, pues algunas moléculas de ARN son capaces de catalizar reacciones (como la subunidad 16S de los ribosomas en la que reside la actividad peptidil transferasa).[5] [6] También cabe nombrar unas moléculas sintéticas denominadas enzimas artificiales capaces de catalizar reacciones químicas como las enzimas clásicas.[7]
La actividad de las enzimas puede ser afectada por otras moléculas. Los inhibidores enzimáticos son moléculas que disminuyen o impiden la actividad de las enzimas, mientras que los activadores son moléculas que incrementan dicha actividad. Asimismo, gran cantidad de enzimas requieren de cofactores para su actividad. Muchas drogas o fármacos son moléculas inhibidoras. Igualmente, la actividad es afectada por la temperatura, el pH, la concentración de la propia enzima y del sustrato, y otros factores físico-químicos.
Muchas enzimas son usadas comercialmente, por ejemplo, en la síntesis de antibióticos o de productos domésticos de limpieza. Además, son ampliamente utilizadas en diversos procesos industriales, como son la fabricación de alimentos, destinción de vaqueros o producción de biocombustibles.
CLASIFICACION DE LAS ENZIMAS
El nombre de una enzima suele derivarse del sustrato o de la reacción química que cataliza, con la palabra terminada en -asa. Por ejemplo, lactasa proviene de su sustrato lactosa; alcohol deshidrogenasa proviene de la reacción que cataliza que consiste en "deshidrogenar" el alcohol; ADN polimerasa proviene también de la reacción que cataliza que consiste en polimerizar el ADN.La Unión Internacional de Bioquímica y Biología Molecular ha desarrollado una nomenclatura para identificar a las enzimas basada en los denominados Números EC. De este modo, cada enzima queda registrada por una secuencia de cuatro números precedidos por las letras "EC". El primer número clasifica a la enzima según su mecanismo de acción. A continuación se indican las seis grandes clases de enzimas existentes en la actualidad:
- EC1 Oxidorreductasas: catalizan reacciones de oxidorreducción o redox. Precisan la colaboración de las coenzimas de oxidorreducción (NAD+, NADP+, FAD) que aceptan o ceden los electrones correspondientes. Tras la acción catalítica, estas coenzimas quedan modificadas en su grado de oxidación, por lo que deben ser recicladas antes de volver a efectuar una nueva reacción catalítica. Ejemplos: deshidrogenasas, peroxidasas.
- EC2 Transferasas: transfieren grupos activos (obtenidos de la ruptura de ciertas moléculas) a otras sustancias receptoras. Suelen actuar en procesos de interconversión de monosacáridos, aminoácidos, etc. Ejemplos: transaminasas, quinasas.
- EC3 Hidrolasas: catalizan reacciones de hidrólisis con la consiguiente obtención de monómeros a partir de polímeros. Actúan en la digestión de los alimentos, previamente a otras fases de su degradación. La palabra hidrólisis se deriva de hidro → 'agua' y lisis → 'disolución'. Ejemplos: glucosidasas, lipasas, esterasas.
- EC4 Liasas: catalizan reacciones en las que se eliminan grupos H2O, CO2 y NH3 para formar un doble enlace o añadirse a un doble enlace. Ejemplos: descarboxilasas, liasas.
- EC5 Isomerasas: actúan sobre determinadas moléculas obteniendo o cambiando de ellas sus isómeros funcionales o de posición, es decir, catalizan la racemización y cambios de posición de un grupo en determinada molécula obteniendo formas isoméricas. Suelen actuar en procesos de interconversión. Ejemplo: epimerasas (mutasa).
- EC6 Ligasas: catalizan la degradación o síntesis de los enlaces denominados "fuertes" mediante el acoplamiento a moléculas de alto valor energético como el ATP. Ejemplos: sintetasas, carboxilasas
COFACTORES
Un ejemplo de una enzima que contiene un cofactor es la anhidrasa carbónica, en la cual el zinc (cofactor) se mantiene unido al sitio activo, tal y como se muestra en la figura anterior (situada al inicio de la sección "Estructuras y mecanismos").[48] Estas moléculas suelen encontrarse unidas al sitio activo y están implicadas en la catálisis. Por ejemplo, la flavina y el grupo hemo suelen estar implicados en reacciones redox.
Las enzimas que requieren un cofactor pero no lo tienen unido son denominadas apoenzimas o apoproteínas. Una apoenzima junto con cofactor(es) es denominada holoenzima (que es la forma activa). La mayoría de los cofactores no se unen covalentemente a sus enzimas, pero sí lo hacen fuertemente. Sin embargo, los grupos prostéticos pueden estar covalentemente unidos, como en el caso de la tiamina pirofosfato en la enzima piruvato deshidrogenasa. El término "holoenzima" también puede ser aplicado a aquellas enzimas que contienen múltiples subunidades, como en el caso de la ADN polimerasa, donde la holoenzima es el complejo con todas las subunidades necesarias para llevar a cabo la actividad enzimática.
COENZIMAS
Las coenzimas son pequeñas moléculas orgánicas que transportan grupos químicos de una enzima a otra.[49] Algunos de estos compuestos, como la riboflavina, la tiamina y el ácido fólico son vitaminas (las cuales no pueden ser sintetizados en cantidad suficiente por el cuerpo humano y deben ser incorporados en la dieta). Los grupos químicos intercambiados incluyen el ion hidruro (H-) transportado por NAD o NADP+, el grupo fosfato transportado por el ATP, el grupo acetilo transportado por la coenzima A, los grupos formil, metenil o metil transportados por el ácido fólico y el grupo metil transportado por la S-Adenosil metionina. |
| COENZIMA NADH |
Las coenzimas suelen estar continuamente regenerándose y sus concentraciones suelen mantenerse a unos niveles fijos en el interior de la célula: por ejemplo, el NADPH es regenerado a través de la ruta de las pentosas fosfato y la S-Adenosil metionina por medio de la metionina adenosiltransferasa. Esta regeneración continua significa que incluso pequeñas cantidades de coenzimas son utilizadas intensivamente. Por ejemplo, el cuerpo humano gasta su propio peso en ATP cada día.
TERMODINAMICA
 Al igual que sucede con todos los catalizadores, las enzimas no alteran el e
Al igual que sucede con todos los catalizadores, las enzimas no alteran el equilibrio químico de la reacción. Generalmente, en presencia de una enzima, la reacción avanza en la misma dirección en la que lo haría en ausencia de enzima, solo que más rápido. Sin embargo, en ausencia de enzima, podría producirse una reacción espontánea que generase un producto diferente debido a que en esas condiciones, dicho producto diferente se forma más rápidamente.
Además, las enzimas pueden acoplar dos o más reacciones, por lo que una reacción termodinámicamente favorable puede ser utilizada para favorecer otra reacción termodinámicamente desfavorable. Por ejemplo, la hidrólisis de ATP suele ser utilizada para favorecer otras reacciones químicas.[52]
Las enzimas catalizan reacciones químicas tanto en un sentido como en el contrario. Nunca alteran el equilibrio, sino únicamente la velocidad a la que es alcanzado. Por ejemplo, la anhidrasa carbónica cataliza su reacción en una u otra dirección dependiendo de la concentración de los reactantes, como se puede ver a continuación:
Si el equilibrio se ve muy desplazado en un sentido de la reacción, es decir, se convierte en una reacción muy exergónica, la reacción se hace efectivamente irreversible. Bajo estas condiciones, la enzima únicamente catalizará la reacción en la dirección permitida desde un punto de vista termodinámico.
INHIBICION
Los inhibidores son moléculas que regulan la actividad enzimática, inhibiendo su actividad. A grandes rasgos, pueden clasificarse en reversibles e irreversibles. Las irreversibles se unen covalentemente a la enzima sin posibilidad de revertir la modificación, siendo útiles en farmacología. Algunos de los fármacos que actúan de este modo son la eflornitina, utilizada para tratar la tripanosomiasis africana,[67] la penicilina y la aspirina.Las reversibles se unen de forma reversible a la enzima, pudiendo clasificarse a su vez, según la forma en que intervienen en la reacción, en competitivas, acompetitivas y mixtas. Habitualmente, por su amplia presencia en multitud de procesos, se habla también de inhibición no competitiva, que en realidad no es más que una variante de la ya mencionada inhibición mixta. Sin embargo, por sus características se suele presentar como opuesta a la competitiva, con la que es comparada frecuentemente.
- En la inhibición competitiva, el sustrato y el inhibidor no se pueden unir a la misma enzima al mismo tiempo, como se muestra en la figura de la derecha.[68] Esto generalmente ocurre cuando el inhibidor tiene afinidad por el sitio activo de una enzima en el cual también se une el sustrato; el sustrato y el inhibidor compiten para el acceso al sitio activo de la enzima.
- En la inhibición acompetitiva el inhibidor no puede unirse a la enzima libre, sino únicamente al complejo enzima-sustrato (ES). Una vez formado el complejo con el inhibidor (EIS) la enzima queda inactiva. Este tipo de inhibición es poco común, pero puede darse en enzimas multiméticas.
- La inhibición no competitiva es una forma de inhibición mixta donde la unión del inhibidor con la enzima reduce su actividad pero no afecta la unión con el sustrato. Como resultado, el grado de inhibición depende solamente de la concentración de inhibidor, independientemente de la concentración de sustrato, con lo que varía el valor de la Vmax aparente. Sin embargo, como el sustrato aún puede unirse a la enzima, el valor de Km no varía.
- En la inhibición mixta, el inhibidor se puede unir a la enzima al mismo tiempo que el sustrato. Sin embargo, la unión del inhibidor afecta la unión del sustrato, y viceversa. Este tipo de inhibición se puede reducir, pero no superar al aumentar las concentraciones del sustrato. Aunque es posible que los inhibidores de tipo mixto se unan en el sitio activo, este tipo de inhibición resulta generalmente de un efecto alostérico donde el inhibidor se une a otro sitio que no es el sitio activo de la enzima. La unión del inhibidor con el sitio alostérico cambia la conformación (es decir, la estructura terciaria) de la enzima de modo que la afinidad del sustrato por el sitio ativo se reduce
- USO DE LOS INHIBIDORES
CINETICA DE Michaelis-Menten
Como las reacciones catalizadas por enzimas son saturables, la velocidad de catálisis no muestra un comportamiento lineal en una gráfica al aumentar la concentración de sustrato. Si la velocidad inicial de la reacción se mide a una determinada concentración de sustrato (representado como [S]), la velocidad de la reacción (representado como V) aumenta linealmente con el aumento de la [S], como se puede ver en la figura. Sin embargo, cuando aumentamos la [S], la enzima se satura de sustrato y alcanza su velocidad máxima (Vmax), que no sobrepasará en ningún caso, independientemente de la [S].
El modelo de cinética michaeliana para una reacción de único sustrato se puede ver en la figura de la izquierda. Primeramente, tiene lugar una reacción química bimolecular entre la enzima E y el sustrato S, formándose el complejo enzima-sustrato ES. Aunque el mecanismo enzimático para una reacción unimolecular puede ser bastante complejo, existe una etapa enzimática limitante que permite que el mecanismo sea simplificado como una etapa cinética única cuya constante es k2.
- (Ecuación 1)
A bajas concentraciones de sustrato, la enzima permanece en un equilibrio constante entre la forma libre E y el complejo enzima-sustrato ES. Aumentando la [S] también aumentamos la [ES] a expensas de la [E], desplazando el equilibrio de la reacción hacia la derecha. Puesto que la velocidad de reacción depende de la [ES], la velocidad es sensible a pequeños cambios en la [S]. Sin embargo, a altas [S], la enzima se satura y solo queda la forma unida al sustrato ES. Bajo estas condiciones, la velocidad de la reacción (v ≈ k2[E]tot = Vmax) deja de ser sensible a pequeños cambios en la [S]. En este caso, la concentración total de enzima ([E]tot) es aproximadamente igual a la concentración del complejo ES:
- (Ecuación 2)
La constante de Michaelis Km se define como la concentración a la que la velocidad de la reacción enzimática es la mitad de la Vmax. Esto puede verificarse sustituyendo la concentración de sustrato por dicha constante ([S] = Km). Si la etapa limitante de la velocidad de la reacción es lenta comparada con la disociación de sustrato (k2 <<< k1), la constante de Michaelis Km será aproximadamente la constante de disociación del complejo ES, aunque sea una situación relativamente rara.
La situación más común, donde k2 > k1, es denominada cinética de Briggs-Haldane.[9] La ecuación de Michaelis-Menten aún se mantiene bajo estas condiciones más generales, como puede derivarse de la aproximación del estado estacionario. Durante el período inicial, la velocidad de la reacción es más o menos constante, indicando que la [ES] también se mantendrá constante:
EJEMPLOS DE ENZIMAS:
- Bromelaína, extraída de la piña
- Papaína, extraída de la papaya
- Pepsina 1:3000, enzima que digiere proteínas
- Tripsina, enzima que digiere proteínas
- Lipasa, enzima que digiere grasas
- Pancreatina. Es generada por el páncreas y contiene los tres tipos de enzimas para digerir las grasas (lipasa), los carbohidratos (amilasa) y las proteínas (proteasa). 2520 unidades USP de Proteasa, 2625 unidades USP de Amilasa, 210 unidades USP de Lipasa.



 (en
(en  (en
(en 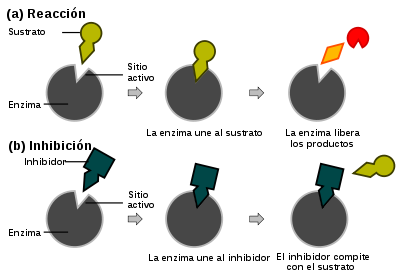


 puede ser bastante complejo, existe una etapa enzimática limitante que permite que el mecanismo sea simplificado como una etapa cinética única cuya constante es k2.
puede ser bastante complejo, existe una etapa enzimática limitante que permite que el mecanismo sea simplificado como una etapa cinética única cuya constante es k2. (Ecuación 1)
(Ecuación 1)

 (Ecuación 2)
(Ecuación 2)




No hay comentarios:
Publicar un comentario